石灰の基礎知識
石灰の種類 編
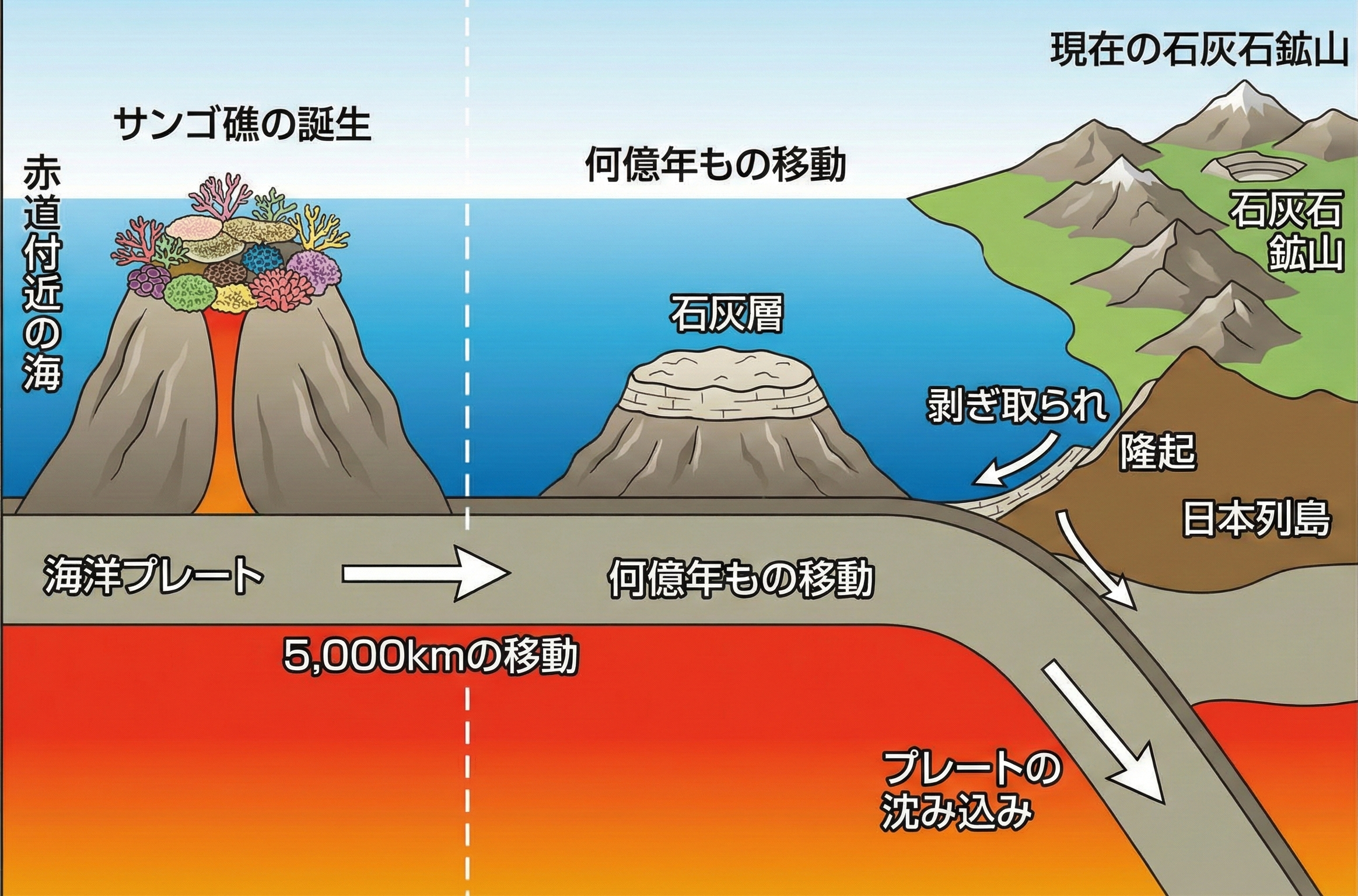
日本は石灰の宝庫!
石灰の循環と仕組み。
石灰の変化
石灰石
太古のサンゴなどが堆積してできた鉱物資源。
主成分はCaCO₃(炭酸カルシウム)。
原料として採掘・使用されます。
粉砕したものは「重質炭酸カルシウム」と呼ばれます。
生石灰(せいせっかい)
焼成により二酸化炭素が抜け、CaO(酸化カルシウム)になった状態。
非常に反応性が高く、水に触れると強い熱を発しながら膨張します。
消石灰(しょうせっかい)
生石灰に水を反応させたCa(OH)₂(水酸化カルシウム)。
化学的に安定した白い微粉末で、強いアルカリ性を示すのが特徴です。
軽質炭酸カルシウム
消石灰に再びCO₂が反応したもの。
原料の石灰石と同じ成分に戻りますが、純度と機能性が高まっています。
生石灰(せいせっかい)
石灰石を徹底した温度管理のもとで焼成し、不純物を極限まで取り除いた高純度な製品です。
最大の特徴は「高い吸湿性」と「水と反応して高熱を出す」こと。
この化学反応は、工業用原料としてもエネルギー源としても重要な役割を果たしています。
CaCO₃(炭酸カルシウム)- CO₂ = CaO(酸化カルシウム)

食品用乾燥剤はもちろん、工業分野ではアルコールや溶剤の脱水剤としても使用され、品質保持に貢献しています。

駅弁や防災食を温める加熱剤として、火を使わずに安全に熱エネルギーを生み出すことができます。
消石灰(しょうせっかい)
生石灰に水を加え、熟成させることで生まれる白く微細な粉末です。
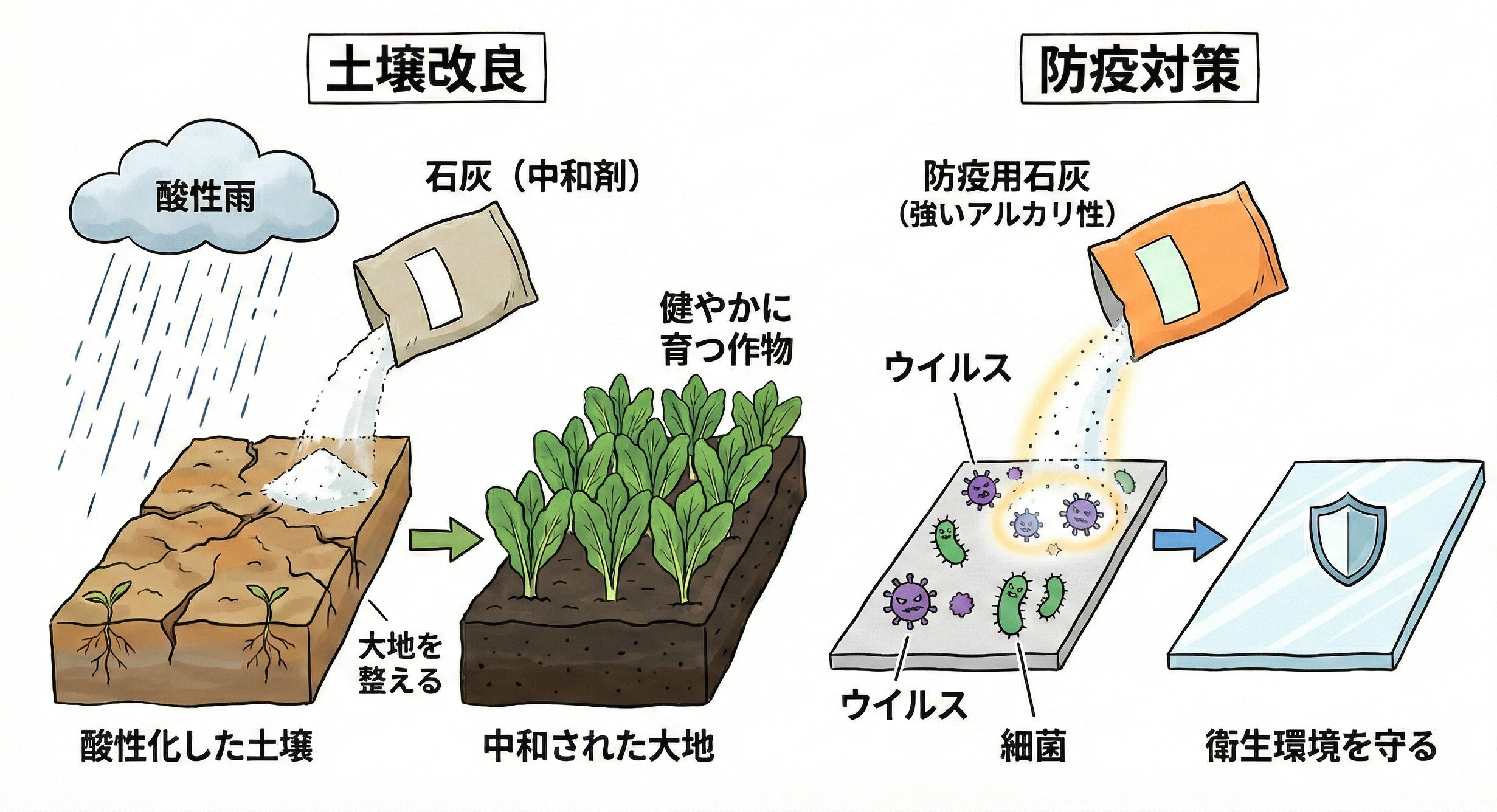
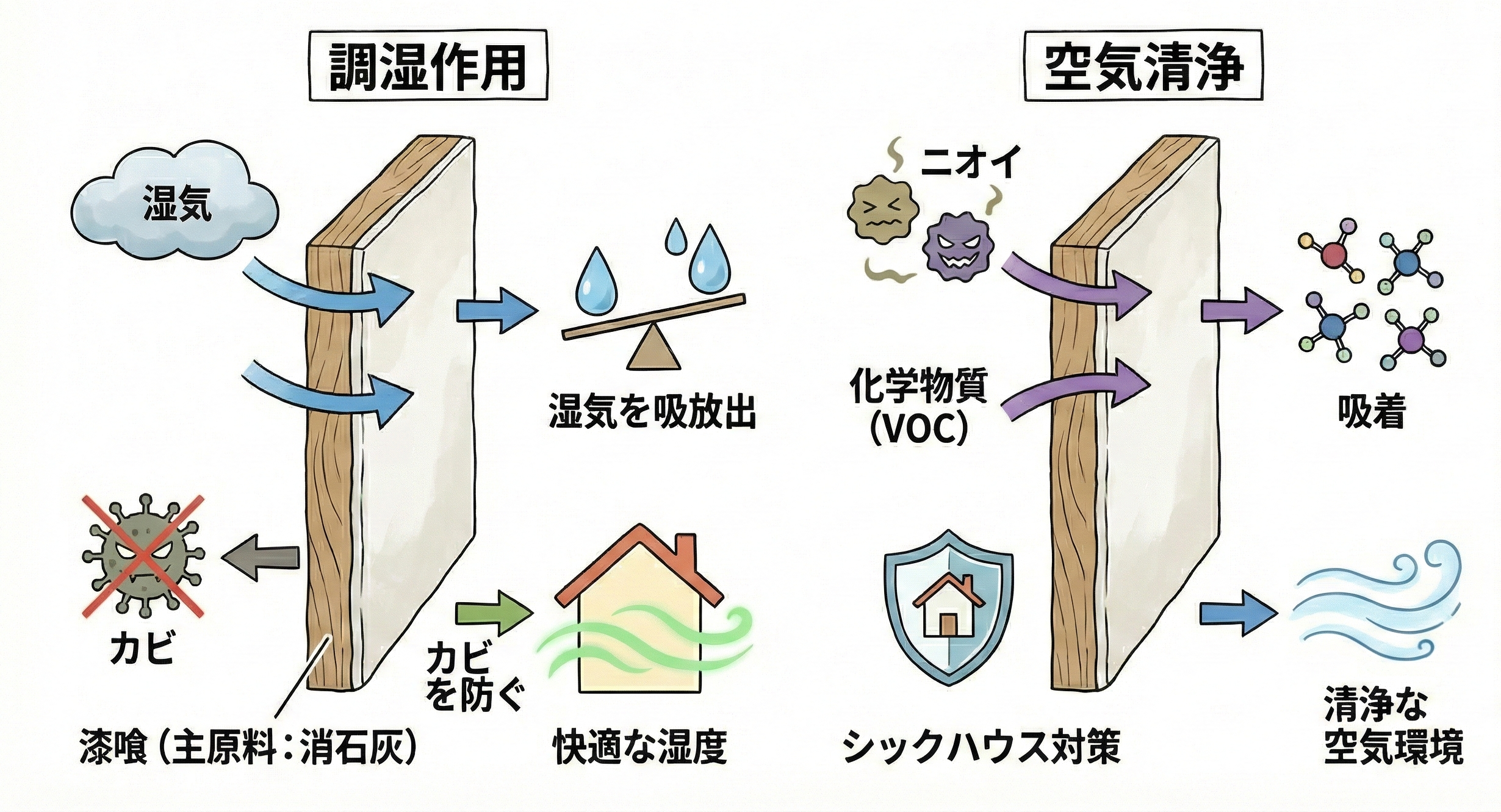
水に溶けると「強いアルカリ性」を示し、この性質が環境保全や衛生管理に役立っています。
CaO(酸化カルシウム)+ H₂O = Ca(OH)₂(水酸化カルシウム)

ゴミ焼却場の有害な酸性ガス(HCl等)の中和除去や、工場排水のpH調整剤として、クリーンな環境を守り続けています。

鳥インフルエンザ等のウイルス消毒や、酸性土壌の改良剤として、農業と私たちの食の安全を足元から支えています。
比較表
| 生石灰 (CaO) | 消石灰 (Ca(OH)₂) | |
|---|---|---|
| 作り方 | 石灰石を焼成 | 生石灰に加水 |
| 特徴 | 吸湿・発熱 | 強いアルカリ性 |
| 形状 | 塊・顆粒・粉末 | 微粉末 |
| 主な役割 | 乾燥・脱水・熱源 | 中和・浄化・消毒 |
井上石灰工業の強み
私たちは、140年以上の歴史の中で培った技術により、
原料の選定から品質管理に至るまでこだわり抜いています。
「高純度・高機能な石灰」は、
食品・医療・工業あらゆる分野の課題解決に貢献します。
石灰の品質 編
なぜ、日本の石灰石は
世界有数の「高品質」なのか。
環境・未来 編
石灰は「自然に還る」
循環型の環境素材。